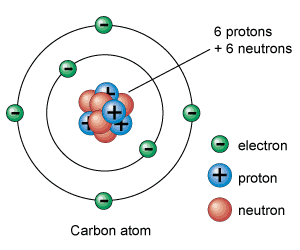
 Generalmente, estas partículas subatómicas con las que están formados los átomos son tres: los electrones, los protones y los neutrones. Lo que diferencia a un átomo de otro es la relación que se establecen entre ellas.
Generalmente, estas partículas subatómicas con las que están formados los átomos son tres: los electrones, los protones y los neutrones. Lo que diferencia a un átomo de otro es la relación que se establecen entre ellas.Los electrones tienen una carga negativa y son las partículas subatómicas más livianas que tienen los átomos. La carga de los protones es positiva y pesan unas 1.836 veces más que los electrones. Los únicos que no tienen carga eléctrica son los neutrones que pesan aproximadamente lo mismo que los protones.
Los protones y neutrones se encuentran agrupados en el centro del átomo formado el núcleo atómico del átomo. Por este motivo también se les llama nucleones. Los electrones aparecen orbitando alrededor del núcleo del átomo.
De este modo, la parte central del átomo, el núcleo atómico, tiene una carga positiva en la que se concentra casi toda su masa, mientras que en el escorzo a, alrededor del núcleo atómico, hay un cierto número de electrones, cargados negativamente. La carga total del núcleo atómico (positiva) es igual a la carga negativa de los electrones, de modo que la carga eléctrica total del átomo sea neutra.
Esta descripción de los electrones orbitando alrededor del núcleo atómico corresponde al sencillo modelo de Bohr. Según la mecánica cuántica cada partícula tiene una función de onda que ocupa todo el espacio y los electrones no se encuentran localizados en órbitas aunque la probabilidad de presencia sea más alta a una cierta distancia del núcleo.
http://energia-nuclear.net/definiciones/atomo.html
